中国粉体网讯 锂离子电池:是一种二次电池(充电电池),主要依靠锂离子在正极和负极之间移动来工作。锂系电池分为锂电池和锂离子电池。手机和笔记本电脑使用的都是锂离子电池,通常人们俗称其为锂电池。而真正的锂电池是一类由锂金属或锂合金为负极材料、使用非水电解质溶液的电池。由于锂金属的化学特性非常活泼,使得锂金属的加工、保存、使用,对环境要求非常高。所以,锂电池没有得到长期应用。
锂离子电池的发展历程
锂离子电池产生阶段(1950—1980年)
1970年埃克森的M.S.Whittingham采用硫化钛作为正极材料,金属锂作为负极材料,制成首个锂电池。
日本的三洋公司在1975年开发了LiMnO2电池(锂电池),随后锂二次电池开始量产。这种电池负极采用的是金属锂材质,在充放电过程中容易造成电池短路,引起爆炸等安全性问题,些因素无疑限制了锂离子电池的发展。
锂离子电池快速发展阶段(1980—2000年)
1980年Armand提出以可嵌入式材料替代金属锂作为电池负极材料。
1982年伊利诺伊理工大学的R.R.Agarwal和J.R.Selman发现锂离子具有嵌入石墨的特性,人们尝试利用锂离子嵌入石墨的特性制作充电电池。首个可用的锂离子石墨电极由贝尔实验室试制成功。
1992年日本SONY公司最早开发了商业化的锂离子电池。用LiCoO2作为正极材料和碳作为负极材料,在充放电过程中,没有金属锂存在,只有锂离子,大地推动了锂离子电池商业化的进程。
锂离子电池发展的新阶段(2000年至今)
2000年以后锂离子电池的发展逐渐成熟,直至今日锂离子电池在生活中的应用随处可见,小到手机、笔记本电脑,大到电动汽车、航空领域等,极材料与负极材料也越来越丰富。
锂离子电池性能特点
锂离子电池由于其比能量高、无记忆效应、工作电压高、安全、寿命长及循环性能好等优点,被广泛用于电动汽车、电子设备以及储能设备中。
①比能量高
锂离子电池的质量比能量是酸铅电池的4倍,是镍镉电池的2倍以上。也就是说同样储能条件下体积仅是镍镉电池的一半。所以现代化的便携式电子设备使用锂离子电池可以减轻重量,缩小体积。
②工作电压高
一般单体锂离子电池的电压约为3.6V,有些可达到4V以上。是铅酸电池的2倍,镍镉
电池和镍氢电池的3倍。
③循环使用寿命长
80%DOD(放电深度)充放电可达1200次以上,远远高于其他电池,具有非常高的经济实用性。
④自放电小
一般月均放电率在10%以下,Ni-Cd电池为25-30%,Ni-MH电池为30-35%,不到镍镉电池和镍氢电池的一半。
⑤绿色、实用
电池材料不会造成环境污染,被称为“绿色电池”;具有较好的加工灵活性,可制成各种形状的电池;工作温度为-25~45℃,随着电解液和正极的改进,期望能扩宽到-40~70℃。
表1四种二次电池性能比较

锂离子电池的工作原理

当对电池进行充电时,正极失去电子,锂离子从正极材料的晶格脱出,进入电解池,穿过隔膜后运动到负极。同时到达负极一侧的锂离子嵌入到负极材料,此外电子也经由外电路到达负极,负极得到的电子与嵌入的锂离子结合形成锂碳层间化合物。
当电池放电时,发生相反的过程。由此可见,在充放电过程中,锂离子和电子的运动方向是一致的。不同的是锂离子是在电路中往返运动,而电子则是经过外电路传输。
锂离子电池材料的分类
商业化使用的锂离子电池的正极材料按结构可以分为三类:
六方层状晶体结构的 LiCoO2
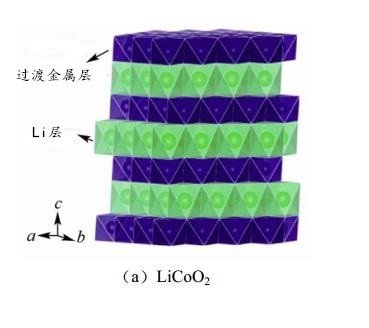
立方尖晶石晶体结构的 LiMn2O4
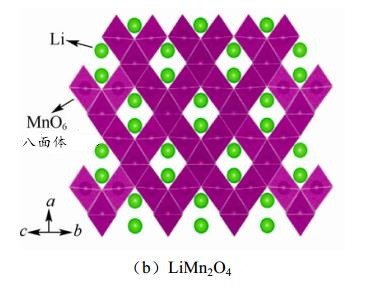
正交橄榄石晶体结构的 LiFePO4
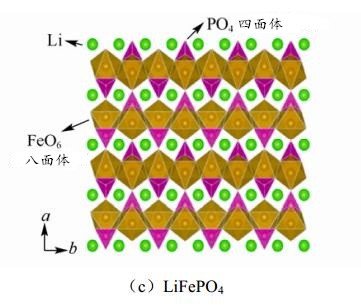
负极材料分类:
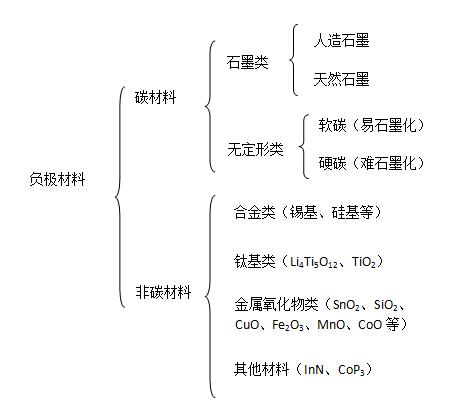
电解质分类:
电解质盐种类很多,主要有LiPF6、LiClO4和LiAsF6等。
LiPF6:离子电导率较好、稳定性也不错而且对环境污染较轻,是目前首选的锂离子电池电解质,缺点是价格较高。
LiClO4:是早期研究的电解质锂盐,具有很强的氧化性,容易引起电池安全性问题,目前使用较少。
LiAsF6:导电性较好,但是As元素的毒性限制了它的使用。
锂离子电池具有明显优于传统二次电池的特点,但在实际应用中也还是存在一些缺点,例如能量密度低、倍率性能不够等问题。所以下一步锂离子电池的发展将重点在提升能量密度的方向,其中包括采用金属锂作为负极材料、嵌入式化合物作为正极材料、聚合物固态电解质和采用锂-硫电池、锂-空气电池等。