�й�������Ѷ ������ӵ�ظ�����������ʯī�������������������۱��������ߣ���������������ܶ�����ӵ�ط�չ����Ҫ��Ŀǰ�о��϶�ĸ��������й�����ϡ��������ϡ����ɽ����������Լ��Ͻ�����ϵȡ�Fe2O3���ڹ��ɽ����������һ�֣����нϸߵ��������������ҳɱ��͡������Ѻá���Դ�ḻ���ܵ��㷺��ע��
1��Fe2O3���ṹ
���������������ͣ�������-Fe2O3����-Fe2O3����-Fe2O3����-Fe2O3�����У���-Fe2O3�����ȶ��Ĵ�����̬����Ȼ�索�����ߣ��׳Ƴ�����Fe2O3Ϊ����ṹ����ṹ��ͼ1��ʾ��
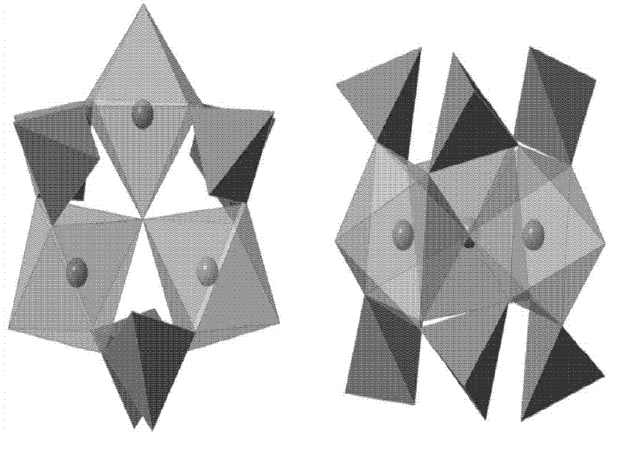
ͼ1 Fe2O3����ṹͼ[1]
2��Fe2O3����﮻���
Fe2O3��Ϊ���ɽ�����������ת���������ϣ��䴢﮻�����ת���ͻ��ƣ�Fe2O3���������ڳ�ŵ������������ӷ���������ԭ��Ӧ������Ƕ﮹���ʱ�����ɽ����������е�����﮽������Li2O��������﮹���ʱ��Li2O�ֱ���ԭΪﮣ����ɽ����������������ɣ��Ӷ����Li+��Ƕ����ѳ���ת�����̿���������ʽ�ӱ�ʾ[2]��
Fe2O3 +xLi+ +xe- ��LixFe2O3
LixFe2O3 +(2-x) Li+ +(2-x) e- ��Li2Fe2O3
Li2Fe2O3 +4Li+ +4e-↔2Fe+3Li2O
3��Fe2O3���Ʊ�����
��1����������
�������������ܽ���λ����Һ�м����������������Һ��ˮ����̣���þ��ȳ����Ľ��������ӣ����Ʊ��õ�ǰ����ij�����������ˮ������������תΪ��ϸ�ķ�ĩ״���������ù�����������ͨ�����Ʒ�Ӧ���¶ȡ���Ӧ���ʵ�Ũ�ȡ���Һ��pHֵ�Ͷ��մ���ʱ������õ���ͬ��ò����-Fe2O3��������[3]���ַ����ϳɹ��ռ��ŵ����ڿ���ֱ��ͨ����Һ�еĻ�ѧ��Ӧ�õ��ߴ��С�Ҿ��ȵ���������Lima��[4]��Fe(NO3)3��9H2OΪ��Դ�����Ǻ�����Ϊ������Լ���ͨ�����������Ʊ������ṹ����-Fe2O3��ʵ���������ͬŨ�ȵı�����Լ���Բ��ϳߴ硢��״�����ȷֲ�����Ӱ�졣
��2��ˮ�ȷ�
ˮ�ȷ������ܷ����Ӧ���У���ˮΪ�ܼ����ڸ��¸�ѹ�����£���Ӧ�����ѧ��Ӧ�γ��������Ĺ��̡�ˮ�ȷ��ܶԷ�Ӧ�����ܼ���ǰ�����¶ȡ����ͷ�Ӧʱ���ˮ�����������е��ڣ����Ʒ�Ӧ��ijɺ˺��������̡�������ˮ�ȷ�Ҳ��һ���ľ����ԣ�����������Ҫ��ϸߣ���Ҫ�ڸ��¸�ѹ�½��У�һ������ʵ���Һ�С��ģ�Ʊ����ײ�������ˣ��÷������ʺϴ�����������Su��[5]��FeCl3��ˮ���º�����ʯīΪԭ����180����ˮ�ȷ�Ӧ8Сʱ���ϳ�������Fe2O3��ʯīϩ�ĸ��ϲ��ϣ����ߴ�ԼΪ7nm��Fe2O3�������Ӿ��ȵظ�����GN��Ƭ�ϣ���Ч�ط�ֹ��Fe2O3���������žۡ�ʵ��������ò����ڿ���������ѭ�����ܷ��涼���ֳ��Ϻõ����ԣ��ܹ����ڸ����ܵ�����ӵ�صĸ������ϡ�Zheng��[6]����ˮ�ȷ���Fe(NO3)3��NaFΪԭ����170���·�Ӧ4Сʱ���ϳ��˽����-Fe2O3��������0.2C�ĵ����ܶ��£��״ηŵ������ͳ�������ֱ�Ϊ1012mAh/g��833mAh/g���ھ���100��ѭ��֮������������Ϊ94%����
��3���ܽ�-������
�ܽ�-�����������������ܽ����ܼ��У�ͨ���ض��Ĵ����ֶΣ��γ���һ���ռ�ṹ�������������ȴ����õ�����Ҫ������������ϡ��÷����豸�������������̼����Ʊ������ײ��Ͼ��нϸߵĴ��ȣ����Ʊ�Fe2O3���÷���֮һ��Kopanja��[7]ͨ���ܽ�-����ȼ�շ������ε�SiO2�л�ø߷�ɢ����-Fe2O3��������ͨ�����ַ����Ʊ�����-Fe2O3����������ڴ�ͳ���ܽ�-���������нϸߵĴŻ�ǿ�ȣ��������ڱ���ԭ�Ӽ������������������ı��������������ӡ�H.Cui��[8]ͨ�������ܽ�-�������ϳɵ���ɢ��-Fe2O3����-Fe2O3�� Fe3O4�������ӡ���FeCl2�ͻ����������Ҵ��л�ϣ��ڷе�֮�䷢����Ӧ�����ܽ���Ȼ����ܽ����и��ﴦ����ͨ���ı���������õ���������
��4��ģ�巨
ģ�巨���Է�ΪӲģ�巨����ģ�巨��ģ�巨�ǽ����������������ض��ṹ��Ԥ��ģ���ϣ��Ӷ��õ��ض��ṹ�IJ��
�ܶ��о��߽�Ӳģ�巨Ӧ�����Ʊ�������Ľ�ײ����ϡ�ʹ���ض�����������Ϊ��Ӧ��ǰ������ϣ�����ע���Ӳģ��Ŀ��С�Ȼ����һ���¶��½����ٽᾧ�˻�������������Ӳģ���ϣ��Ӷ��Ʊ����ȶ����͵������Ȼ��Ӳģ����ϸ�ʴ���Ʊ��������ȶ����͵Ľ��״������������ϡ���ģ�巨һ������л�����������������������ģ�壬�ڽ�������������Ʊ������н���ģ����л����ǰ�������������ܽ����ܼ��С�Ȼ�����Һ�������ȣ��ڼ��ȹ������������κ���ģ���������װ���Ӷ��õ���-�л����Ͻṹǰ������ϣ�ȥ����ģ���õ�����������ǰ������ϡ����Ʊ������У���ģ���ڼ��ȹ�������Ҫ�䵱���ͼ���
��5�����η�
���η�һ����һ�ֻ���ֵ��۵��������Ϊ��Ӧ���ʣ����÷�Ӧ���������о���һ�����ܽ�ȣ�ʹ�÷�Ӧ���������кܿ���ɢ�������ν��г�ֵĽӴ��������ַ�Ӧ��������Ӧ���ܼ��������ܽ⣬Ȼ������ϴ�ӻ������Ҫ�IJ���÷����ڷ�Ӧ�����кϳ��¶����Խ��ͣ����������˷�Ӧʱ�䣬�������������ڡ�
�����ϼ��ַ����⣬Fe2O3���Ʊ����й����սᷨ�������Ƚⷨ����ķ��ȡ�
4��Fe2O3�����������ڵ����⼰�Ż�����
Fe2O3��Ϊ��������ʱӵ�нϸߵ����۱�����������Ҳ�������Ե�ȱ�㡣��һ��������������⣬�ڳ�ŵ������Fe2O3�����ᷢ�����Ե�����仯�����µ������˥����ѭ�����ܲ�ڶ�����Fe2O3���������Բ�缫��Ӧ�Ŀ�����Ҳ�ͣ����µ缫�ڸ߱��������ܽϲ
������Fe2O3�������ϵ����ܣ����Ż����������¼��֣�
��1����������
���ṹ�ܹ�����Li+�Ĵ�����룬�����ܹ��õ缫���Ϻ͵��Һ֮��Ӵ�����֣�ͬʱҲ�ܻ���Li+Ƕ��ʱ���ϵĽṹ�仯�����ṹ��Fe2O3�ж��֣��������������������װ�������Ƭ�ȵȡ�
Tian��[9]�����ܼ��ȵķ��������Ȼ���Ϊ��Դ���ڷ�Ӧ���и����±����Ƴ��������������������������ͽ���ṹ��������Li+����ɢ·������Ҳ������������Ͷ����������Ļ������ã���������߽總�������Li���/�Ѳ㣬Li1.75+xFe2O3������ͽ���Ҳ����Li�Ĵ������á�����������ĵ绯ѧ���ܴﵽ��Ԥ���Ч�����ڳ�ŵ�����У���������ֳ��˲�����ѭ�����ܣ��������ܶ�Ϊ150mA/gʱ����Ȧ���ŵ�������ﵽ��942.6mAh/g��93Ȧѭ�����Ա�����947.7mAh/g���������У����ŵ�������ѭ�����ܽ��ͣ������ص�ԭֵʱ�������������ԣ�չʾ�����õı���������
Lin��[10]ͨ��ˮ�ȷ�Ӧ�Ƶ����������װ����������װ����ֳ��˲����ĵ绯ѧ���ܣ���0.2C�ĵ����£�30Ȧ�ij�ŵ�ѭ���ŵ������Ϊ900mAh/g����0.5C�ĵ����£���90Ȧ��Ȼ����970mAh/g�ķŵ�����������������װ��缫���������ܹ�������ֱ��С���������Ľṹ�ص㣬Ϊ�������ɢ�ṩ��һ���̵���ɢ·���������ܹ�����һ����ﮡ�
Wang��[11]���ܼ��Ⱥ��ȴ�����ϵķ������Ƚ��Ȼ������Ҵ����ڸ��¸�ѹ�Ļ����±�����Сʱ���õ�������ǰ���壬Ȼ��������գ��õ�����������Ƭ����������Ƭ���ֻ��15-30nm�����Ų����ij�ѭ���������ڵ����ܶ�Ϊ100mA/g�������º�����ŵ���ԣ���Ȧ�ŵ������Ϊ1751mAh/g����Ȧ����Ч�ʴﵽ72.3%��ѭ��10Ȧ�ŵ������������Ȧ��91.3%�����ֿ���˥���������������ڵ���ʵij����ֽ��γ�SEIĤ��Ҳ�����ڵ�س�ŵ�����д��ڲ�����Ľṹ�仯��100��ѭ��֮�ŵ����������1043mAh/g������Ч�ʱ�����98.5%���ϣ���5A/g�Ĵ������500��ѭ��֮��������Ȼ������578mAh/g��
��2�����Ӹ���
���Ӹߵ�����ϣ��ܸ�����������еĵ��ӵ絼�ԣ����������̼��ʯīϩ��̼�����ȡ���ά�ṹ���Ը������������㹻��Ŀռ�������������ͣ�Wang��[12]���ò��ӵķ���������ά�ṹ��״�ṹ��������Դ����ԭ����ͬêһ�����˹̶���Ч�������������������ܵ���״�ṹ�ϣ���һ�ֿ����о��ĸ�Ч�������ϡ����Ŷ����Ȳ����ܽ������ķ������Ʊ���������ʯīϩ����״���Ͻṹ���̶������ȴ������������ӽ�ȥ�����ֽṹ�ڳ�ѭ����ӵ���ȶ�ѭ�����ܣ���500mA/g�µĴ����ѭ��500Ȧ�ŵ��������Ȼ��1121mAh/g���ȶ���ѭ�����ܹ�����ʯīϩ�Ķ�ṹ����ά����״�ṹ�Լ���Դ�̶���������������͡�
��3�����������������︴��
Fe2O3ͨ�����������������︴�ϣ����ò�ͬ�������Խ������ƻ�����Ҳ�ܹ�������ߵ缫���ϵ����ܡ�Qin��[13]����TBOTΪ��Դ����������������һ��Ǿ�̬�������ѣ��Ʊ�Fe2O3@TiO2����TiO2Ϊ�������ǣ���Fe2O3Ϊ���ġ�TiO2�Dz�����Ч�ظ��Ƶ������ܺͽṹ�ȶ��ԡ����Ŷ������Ȼ�����Һ��ͨ�����������ȴ�����ϵķ����Ʊ����������ˡ�Ȼ����ˮ�ȵķ���������ͬ���������ᶡ����TBOT�����л���Ʊ���Fe2O3@TiO2ǰ���壬Ȼ��������ա����ϲ��ϱ��ֳ�������ĵ绯ѧ���ܣ���0.1C�ĵ�����ѭ����100Ȧ�����ܱ���497.3mAh/g�ķŵ�������������µĺ˿ǽṹ���ֳ�����ĵ绯ѧ������Ҫ������TiO2��ֹFe2O3�������ӵķ���;ۼ�����Fe2O3����仯�������Լ�Fe2O3�˺�TiO2�ǵ�Эͬ���á�
5������
Fe2O3��Ϊ����ӵ���������Ͼ��нϸߵ����۱�������������ԭ�ϳɱ����������ȷ������һ�����ƣ��нϴ�ķ�չDZ��������Ҳ��������������͡�ѭ�����ܲ�����ʵ͵�ȱ�㡣�������ڵ����⣬����������о��������������������ӵ��Ż����Բ��ԣ������绯ѧ���ܣ��Ӷ�ΪFe2O3�������ϵIJ�ҵ��Ӧ�ô���������
�ο����ף�
[1]ʱ��ΰ. Fe2O3�������ϵĸ��Լ���﮵������о�[D].����������ѧ,2019.
[2] Sun M,Sun M,Yang H,et al. Porous Fe2O3 nanotubes as advanced anode for high performance lithium ion batteries[J]. Ceramics International, 2017,43(1):363-367.
[3]�����.����ӵ�������������ϵ��Ʊ�������Ե��о�[D].������ѧ,2020.
[4]LIMA R J S,JESUS J R,MOURA K O,et a1.The role of chelating agents on the structural and magnetic properties of ��-Fe2O3 nanoparticle[J].Journal of Applied Physics,2011,109(12): 123905��123910.
[5] Su J,Cao M,Ren L,et al. Fe3O4-Graphene Nanocomposites with Improved Lithium Storage and Magnetism Properties[J]. Journal of Physical Chemistry C, 2011, 115(30):14469-14477.
[6] Na Z,Chen Y,Deng X,et al. Electrochemical investigation of microporous and mesoporous ��-Fe2O3 particles for lithium-ion batteries[J]. Materials Letters, 2014, 124(jun.1):4-7.
[7] A L K,B I M,C M P,et al. Sol-gel combustion synthesis, particle shape analysis and magnetic properties of hematite (��-Fe2O3) nanoparticles embedded in an amorphous silica matrix - ScienceDirect[J]. Applied Surface Science, 2016, 362.
[8]H.Cui,Y.Liu,W.Ren.Structure switch between ��-Fe2O3, ��-Fe2O3 and Fe3O4 during thelarge scale and low temperature sol-gel synthesis of nearly monodispersed iron oxidenanoparticles [J].Advanced Powder Technology, 2013,24(1): 93-97.
[9]Tian L L,Zhang M J,Wu C,et al.��-Fe2O3 Nanocrystalline Microspheres with Hybrid Behavior of Battery-Supercapacitor for Superior Lithium Storage[J].ACS Applied Materials and Interfaces, 2015,7(47): 26284 26290.
[10]Lin Y M,Abel P R,Heller A,et al, ��-Fe2O3 nanorods as anode material for lithium ion batteries[J].Journal of Physical Chemistry Letters, 2011, 2(22): 2885-2891.
[11]Wang Y,Han J,Gu X,et al.Ultrathin Fe2O3 nanoflakes using smart chemical stripping for high performance lithium storage[J]. Journal of Materials Chemistry,2017,5(35): 18737-18743.
[12]Wang R,XuC,SunJ,etal.Three-dimensional Fe2O3 nanocubes/nitrogen-doped grapheneaerogels: Nucleation mechanism and lithium storage properties [J]. Scientific Reports, 2014,4:1-7.
[13]OinG,Zeng,M,Wu,X,et,al.,Fabrication of Fe2O3@TiO2 core shell nanospheres as anode materials for lithium-ion batteries[J].Joural of Materials Science: Materials in Electronics. 2018,29(15): 12944-12950.
���й��������༭����/������
ע��ͼƬ����ҵ��;��������Ȩ��֪ɾ����