中国粉体网讯 在矿业、制陶业和材料学领域中,氧化铝(化学式Al2O3)又被称为矾土,是一种化学键很强的离子化合物,具有高硬度、高机械强度、耐化学腐蚀、耐磨性好和良好的导热性等优异的特点,在工业上是重要的化工原料。
氧化铝晶体结构的排列方式主要有以下两种:一种是氧原子以六方体堆积排列,另一种是氧原子以立方体堆积排列分布。在这两种晶体结构的排列方式中,铝原子大部分占据八面体的位置,但也有少数占据四面体位置的情况,而只有铝原子占据八面体位置的立方晶系和六方晶系的氧化铝结构最稳定。在此基础上,将Al3+按亚点阵结构划分为各种相,氧化铝晶型参数信息见表。
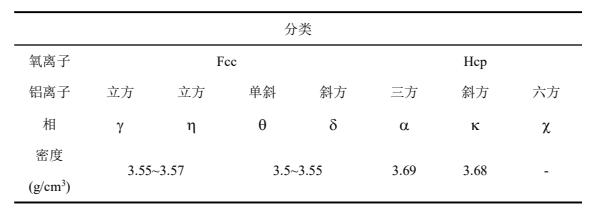
氧化铝相的分类及密度
常见氧化铝性质及应用
目前已经知道的氧化铝共有九种晶体形态,包括α、γ、β、η、δ、θ、χ、κ-Al2O3和无定型相。
(1)α-Al2O3性质及应用
α-Al2O3俗称刚玉,α-Al2O3是白色晶体,是氧化铝晶型中最常见和最稳定的一种,属于三方晶系密排堆积结构。在α-Al2O3晶体结构中,氧离子按照六方紧密堆积排列,呈ABABAB…二层重复,构成若干八面体形状,而铝离子填充在每个八面体间隙中。由于氧离子和铝离子的比例是3:2,使得铝离子无法填满氧离子八面体间隙,只能填充2/3间隙。在该离子晶体结构中,氧离子和铝离子直接的键合作用强,晶格能大,由3个氧离子构成的相邻两个八面体共用一个面,无数个AlO6八面体通过共面结合构成整个大“分子”晶体,因此α-Al2O3晶体比其他晶型Al2O3稳定,使得α-Al2O3晶体的物理化学性质非常稳定,具有良好的机械力学性能和耐腐蚀性。目前α-Al2O3被广泛应用于研磨材料、耐火材料、集成电路基板和结构功能陶瓷等领域。
(2)β-Al2O3性质及应用
β-Al2O3实际上是一种铝酸盐,它是由金属氧化物和氧化铝组成的复合化合物,它的化学式可以近似表达为R2O·11Al2O3或RO·6Al2O3,R2O代表碱金属氧化物(主要是CaO和MgO),RO代表碱土金属氧化物(主要是K2O和Na2O)。
β-Al2O3晶体与α-Al2O3晶体氧原子的紧密堆积排列不同,其具有层状结构,碱金属离子或者碱土金属离子层尖晶石结构单元交替堆积而成,氧离子则按立方紧密堆积排列,金属离子如Na+可以在该平面层内快速扩散,因此β-Al2O3晶体可以导电,是一类重要的固体电解质。因此可利用β-Al2O3来制备钠-硫电池中的固态电解质隔膜材料,还可以起到离子导电和隔离电池阴阳两极的重要作用。除此之外,β-Al2O3还可以用作耐火材料以及电子领域里如用于电子手表、照相机、听诊器和心脏起搏器等器件中。
(3)γ-Al2O3性质及应用
γ-Al2O3是最常用的过渡态氧化铝,在自然界中不存在,其结构中氧离子可以被近似为立方紧密堆积,而铝离子则不规则分布在由氧离子构成的八面体和四面体空隙中,属于尖晶石结构。γ-Al2O3的制备工艺比较简单,其形成温度较低,一般在500~700℃范围内,γ-Al2O3不溶于水通常能够溶解在酸或碱当中。γ-Al2O3晶体晶粒粒径很小,通常在5~10nm。此外,γ-Al2O3粉体还是一种重要的多孔性物质,其比表面积较大,具有吸附功能好、化学反应活性大和催化性好等优点,又被称为活性氧化铝,它的主要用途是作为吸附剂、干燥剂和催化剂的载体,常用于石油化工和环境保护领域。
(4)其它
η-Al2O3属立方晶系,可由拜尔石在一定的升温速率下在400-750℃煅烧得到。它具有和γ-Al2O3相差不大的孔容和比表面积,表面酸性比Al2O3要强,主要用作催化剂的载体。
δ-Al2O3属四方晶系,该材料具有强吸附能力和催化活性,常常被用作吸附剂、干燥剂以及催化剂载体。
θ-Al2O3属单斜晶系,其比表面积和孔容往往介于γ-Al2O3和α-Al2O3之间。
χ-Al2O3属于六角晶系,χ-Al2O3主要用于天然气和石油裂解气的脱水干燥,同时也是水除氟,蒽醌法制备双氧水反应的催化剂。
κ-Al2O3属六方晶系,κ-Al2O3可由三水铝石在800-1150℃煅烧得到,它主要用做耐火材料结合剂、净化剂、吸附剂等。
不同晶型氧化铝的相转变
在不同的晶型中,只有α-Al2O3为稳定的晶相,其他各相都为过渡相,处于热力学不稳定状态,随着温度的升高,不稳定过渡态氧化铝均可转变为稳定的相,这是一种晶格重构的不可逆转变。
要获得稳定的α-Al2O3,需要从开始的原矿筛选、粉末合成到烧结的完善的工艺控制。国内外制备高温氧化铝通常采用以工业氢氧化铝或者工业氧化铝为原料,通过脱水形成过渡相,再在高温下经过多次相态的转换,最终转变为α相的Al2O3。
三水铝石(Al(OH)3)和薄水铝石(AlOOH)是制备α-Al2O3最常用的前驱体。在开始的热处理过程中,氢氧铝以亚稳结构的形式转变为过渡氧化铝,最后以α-Al2O3热力学稳定相结束。另外,薄水铝石在500~550℃的温度范围内失去结构水,转变为γ-Al2O3过渡氧化铝。θ-Al2O3过渡氧化铝到α-Al2O3的转变发生在1050~1200℃的温度范围内。这个过程晶向的转变通过成核和晶粒生长机制发生,并受到晶粒尺寸、化学成分和加热速率等参数的影响。从γ-Al2O3单斜相(d=3.56g/cm-3)到α-Al2O3六方相(d=3.98g/cm-3)的转变伴随着约10%的体积减小,会导致氧化铝密度大幅增加。
工业上通常采用不同的煅烧方式将亚稳定相态γ-Al2O3向α稳定相态转化,制备出不同形貌的α-Al2O3。通过控制不同的煅烧温度、加入不同种类的添加剂、研磨方式等,可以生产出不同形貌的α-Al2O3。通常包括蠕虫状、片状、柱状、类球状、球状、纤维等多种形态的α-Al2O3晶体。
小结:
随着国内陶瓷工业、医药工业、电子工业以及机械行业的快速发展,氧化铝市场需求还有很大发展空间,因此对氧化铝的研究具有深刻意义。而了解和掌握氧化铝的晶体结构和性质是制备氧化铝粉体的重要前提。不同晶型的氧化铝,其应用领域也不尽相同。α-Al2O3是所有氧化铝形态中最稳定的,生产上一般通过控制α-Al2O3晶体的生长环境,制备出不同类型的α-Al2O3晶体,以适应陶瓷、耐火材料及其他新型功能材料对α-Al2O3不同晶体显微结构的需求。
参考来源:
1、胡博强,侯焕焕等.氧化铝晶型变化
2、曹志强,陈昱锟等.α-氧化铝的结构、性质及应用前景
3、张心新.明胶凝胶模板法制备片状纳米.α-Al2O3粉体及机理研究
4、中国粉体网:百科:不同晶型的氧化铝简介
(中国粉体网编辑整理/青黎)
注:图片非商业用途,存在侵权告知删除